CDISC標準ケースカード 調査票入力プログラム

サービス概要
![]() CDASH対応準備はお済みですか?
CDASH対応準備はお済みですか?
背景
1997年にCDISC Clinical Data International Standards Consortiumが発足し、その7年後の2004年にデータセット形式SDTM Ver1.0仕様策定がリリースされ、同年FDAがCDISC(CDASH)データ申請受付を開始しました。
日本でも申請電子データにおいて様々な検討がなされ、ようやく2016年からCDISC(CDASH)による電子データ申請が義務化される事となりました。
様々なお客様の声
|

|
そんなお困りごとを一掃
弊社は必要な時に変換したい分だけ、積み重ねてきた技術とノウハウで対応します。
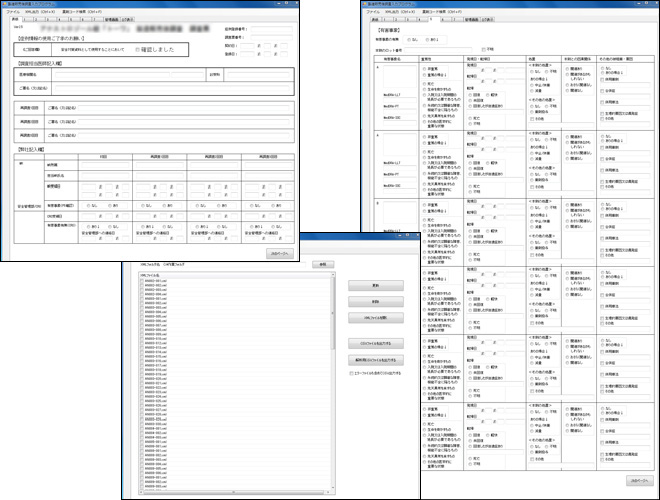
CDASH対応調査票(症例報告書(CRF)ケースカード)入力プログラムは、世界標準のXMLをベース保存形式とした個別開発型プログラムです。
(従来Office Access での .accdb や .accdrといったデータ保存形式では、アプリケーション依存による困り事が多くあったことを踏まえての選択です。)実践で鍛えたXML技術開発力をもってサポートいたします。
入力後の患者データは、CDISC標準 CDASH仕様は勿論、ODM・SDTMへの個別及びマージデータ、必要項目抽出のデータ・セットでの出力が可能です。
対象:適正対象症例数が800症例以下
(想定外の記入に合わせた柔軟な個別プログラム修正が多い案件向けに最適なスキームです。)
*本プログラムは、すでにCDASH標準対応にて導入実績があります。
*パッケージ製品ではありません。調査票に合わせた入力画面のカスタマイズが必要です。
作業フロー
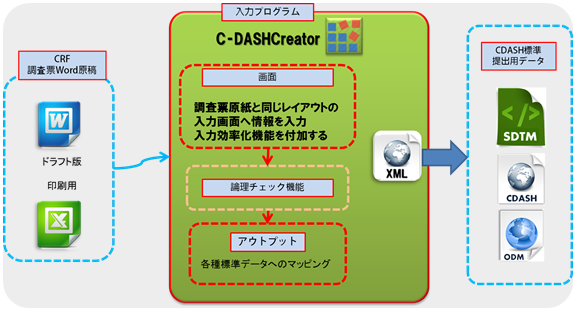
CDASHの基となるXMLを操るプロフェッショナルの視点から、CDASH調査票入力プログラムをご提供します。
貴社にてWord等で作成いただいた調査票をお送りいただくだけで、
CDASH対応調査票入力プログラム開発を請け負うサービスです。
手順
STEP1 CDASH標準の変数名表を基に調査票を作成
STEP2 構造定義書作成
STEP3 ロジカルチェック仕様書作成
STEP4 画面設計
STEP5 内部プログラム
STEP6 個別データのXML管理
STEP7 XMLデータのマージ、抽出により正規化したシートごとへのCSVへ出力
納品物
構造定義書
入力仕様書
調査票入力プログラム
(ロジカルチェックは別途ご用意下さい)
上記開発プログラムでCDASH申請データ作成の効率化支援を行います。